Вітаю Вас Гість
Головна | Реєстрація | ВхідМедична скарбниця
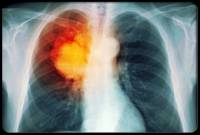
1:18 PM Лікування раку легень | |
Лікування раку легень У випадках карциноми in situ (стадія 0) добрий
лікувальний ефект (90-100 %) отримано при застосуванні фотодинамічної лазерної
терапії. Хірургічне лікування є методом вибору в
пацієнтів, які мають І-ІІ стадію раку. На жаль, І-ІІ стадія діагностується лише
в 15-20 % пацієнтів. Крім того, ще в доопераційний період необхідно чітко
визначитися з такими факторами як резектабельність та операбельність. Якщо
наявні ці дві умови, то хірургічне лікування раку ІА стадії буває успішним в
65-80 % випадків, ІВ стадії - в 50 %, а ІІА-В стадії - в 30-40 % випадків.
Вважається обов'язковим морфологічне дослідження лімфатичних вузлів найближчих
колекторів (N1, N2) із метою оцінки реального поширення процесу й планування
ад'ювантних методів терапії. Основні типи операцій, які
виконуються при раку легень І стадії: лобектомія, білобектомія, муфтоподібна
резекція головного бронха, бронхопластична лобектомія, пневмонектомія; в
окремих випадках крайова резекція або сегментектомія (при цьому рецидиви в три
рази частіше). Післяопераційна 30-денна летальність при лобектомії становить ~
3 %, пневмонектомії -6-8 %, сегментектомії і крайовій резекції - 0,4-1,4 %. У
зв'язку з тим, що віддалені результати виживання після лобектомії і
пульмонектомії однакові, лобектомія може бути операцією вибору, якщо це
технічно можливо. Сучасна технологія
відеоторакоскопічної хірургії (VATS) дозволяє виконувати крайову резекцію, лобектомію і,
навіть, пульмонектомію з мінімальними післяопераційними ускладненнями. Паліативні методи. У випадку центральної
карциноми з обструкцією бронха, для реканалізації просвіту бронха і відновлення
функції ателектазованої частки легені застосовують фотодинамічну лазерну
терапію або лазерну (Nd:YAG) бронхоскопічну фотокоагуляцію пухлини з
встановленням ендобронхіального стента. Ознаки нерезектабельності раку
легень: віддалені метастази
(включаючи протилежну легеню); плевральний випіт; синдром верхньої порожнистої
вени; метастази в надключичні або шийні лімфовузли, чи в контралатеральні
медіастинальні (N3); ураження нервів
(поворотного, гортанного, діафрагмального); проростання у стінку трахеї. Рак Пенкоста (T3N0M0, ІІВ стадія):
починають лікування з променевої терапії (або чи разом з хіміотерапіэю), потім
операція та хіміотерапія. Ад'ювантна терапія На І-й стадії післяопераційна
ад'ювантна променева чи хіміотерапія не покращує віддалених результатів
порівняно з одним лише хірургічним лікуванням. У пацієнтів із плоскоклітинною
карциномою ІІ стадії післяопераційна променева терапія зменшує появу рецидивів,
однак не покращує загального виживання. Ад'ювантна післяопераційна хіміотерапія (Cyclophosphamide, Doxorubicin, Cisplatin) у випадках аденокарциноми і крупноклітинного раку ІІА-В i IIIA стадії віддаляє час появи рецидивів і покращує загальне виживання. У половини пацієнтів рецидиви і метастази виникають у перші два роки після операції. У зв'язку з цим розробляються
методи неоад'ювантної і протоад'ювантної хіміотерапії резектабельного раку на
стадії ІВ, ІІА-В і ІІІА. При цьому пацієнти отримують два курси доопераційної
хіміотерапії (Mitomycin, Ifosfamide, Cisplatin або Paclitaxel, Carboplatin) і три курси в
післяопераційний період (у випадках T3 і N2 комбінують з променевою терапією). Трьохрічні
результати такого комбінованого лікування кращі, ніж лише хірургічного. Лікування недрібноклітинного раку
на стадії ІІІА є складним і суперечливим. Якщо пухлина резектабельна, то
починають із периопераційної хіміотерапії (Cyclophosphamide, Etoposide, Cisplatin), після цього
виконують операцію. Дворічне виживання при такому комбінованому лікуванні
досягає 60 %, проти 25 % при застосуванні лише хірургічного методу. У тих
випадках, коли операція не планується, призначають хіміопроменеву терапію. Пацієнтам із пухлинами ІІІВ і ІV стадій застосовують
лише променеву, хіміотерапію і підтримуюче лікування. Недрібноклітинна
карцинома є однією з найбільш хіміорезистентних пухлин її чутливість до окремих
цитостатиків (Mitomycin, Vindesin, Cisplatinum, Ifosfamid, Vinblastin) становить лише
18-27 %, а при комбінації двох-трьох хіміопрепаратів зростає до 40 %. Променева терапія, яка ще
донедавна була домінуючою, поступається тепер комбінованому лікуванню. При
цьому спочатку призначають кілька курсів хіміотерапії (від двох до восьми),
вибираючи одну з комбінацій хіміопрепаратів (Gemcitabine - Cisplatin, Cisplatin - Vinblastine, Docetaxel - Cisplatin, Docetaxel - Gemcitabine -Vinorelbine, Vinorelbine - Gemcitabine,
Paclitaxel - Gemcitabine, Cisplatin -Vindesine, Cisplatin - Irinotecan), потім - променеву терапію (сумарна доза 60 Гр-екв).
Кращі результати променевої терапії отримані при застосуванні методики
гіперфракціонування дози. Хоча є рандомізоване дослідження, при якому виявлено,
що короткотермінова (прискорена) паліативна радіотерапія (двома сеансами по
8,5 Гр-екв) мала такий же ефект, як і пролонгований курс. Сучасні лінійні прискорювачі
дозволяють використовувати методику конформальної променевої терапії (3D-CRT) з підведенням
максимальної дози (70 Гр-екв) до пухлини при мінімальному променевому
навантаженні на здорові тканини. У випадку невеликих
ендобронхіальних карцином добрі результати отримано при застосованні поєднаної
променевої терапії: дистанційної (до 40 Гр-екв) і ендобронхіальної
брахітерапії (до 25 Гр). Джерелом випромінювання для брахітерапії служить Ir192, активна частка якого
(10 Сі) підводиться до пухлини через назотрахеобронхіальний катетер (6-Fr). Період піврозпаду Ir192 становить 74 дні, тому
брахітерапія може тривати до трьох місяців. Комбінована хіміопроменева
терапія (на III стадії) покращує виживання
пацієнтів вдвічі порівняно із використанням лише самої променевої терапії, хоча
віддалені результати є досить скромними: однорічне виживання для двох груп
пацієнтів становить 55 і 40 %, дворічне - 26 і 13 %, трирічне - 23 і 11 %
відповідно. Хіміопроменеву терапію (окремо чи
комбіновано) призначають, враховуючи індекс Карновського. Пацієнти переносять
лікування нормально і без серйозних побічних ускладнень при ІК 80-100 %. Якщо
ІК 30-50 %, то в таких пацієнтів рідко спостерігається ефект від лікування,
навпаки, хіміопроменева терапія ще більш погіршує їхній загальний стан. Тому
перевагу слід надавати паліативній і підтримуючій терапії. Найбільш проблематичне
лікування у пацієнтів з ІК 60-70 %. У них часто виникають ускладнення: анемія,
лейко- і лімфоцитопенія, тромбоцитопенія. Застосування в таких випадках
колонієстимулюючих факторів (Neupogen, G-CSF - гранулоцитарний фактор; Neumega, Oprelvekin - тромбоцитарний
фактор росту та ін.) сприяє добрій толерантності до хіміотерапії. Дрібноклітинна карцинома - одна з
найагресивніших пухлин людського організму, яка без лікування призводить до
смерті через декілька тижнів чи місяців від моменту встановлення діагнозу.
Традиційно дрібноклітинний рак, крім класифікації за TNM, поділяють на обмежений і поширений.
До обмеженого відносять стадії І, II, ША і HIB (T4N0-2M0 без карциноматозного плевриту), тобто ті стадії, на
яких уражається лише одна половина грудної клітки. Поширеним вважається процес
на стадіях IV і IIIB (N3), коли карцинома виходить за межі однієї половини
грудної клітки (віддалені метастази, синдром верхньої порожнистої вени,
злоякісний плеврит, лімфангіт). Карциноми стадії діагностуються
лише у 5 % пацієнтів і вони є потенційними кандидатами для
хірургічного лікування. Якщо в результаті доопераційного обстеження
верифіковано дрібноклітинний рак, то лікування здійснюється за схемою: неоад'ювантна
хіміотерапія (4-6 курсів) в комбінації з променевою терапією (40-55 Гр-екв), потім або чи поєднання операції та
хіміотерапії. Такий режим дозволяє добитись успіху в 50-75 % хворих. Якщо ж дрібноклітинний рак був
встановлений лише після операції, то відразу ж необхідно призначати
хіміотерапію (шість курсів) в поєднанні з променевою терапією. Цитостатики ефективні
при умові, що вони вводяться інтенсивними дозами і регулярно (через кожні три тижні) до одержання оптимального
результату. Повна відповідь на хіміотерапію досягається у половини пацієнтів
із карциномами на стадіях I, II, IIIA. Тривалість життя в середньому становить 14-16 місяців, а 5-річне виживання відмічається лише в 10-18 % пацієнтів. При комбінованій хіміотерапії
віддалені результати кращі, ніж при хірургічному лікуванні чи променевій
терапії, окремо взятих. Стандартна хіміотерапія включає
комбінації таких препаратів: Etoposide - Cisplatin; Cisplatin - Gemcitabine; Irinotecan (Campto) - Cisplatin; Etoposide - Ifosfamide - Cisplatin; Cyclophosphamide - Doxorubicin - Vincristine. Ефективність їх
становить 65-90 % з повною ремісією у 45-75 % пацієнтів з I-ІІ-ША стадіями та у
20-30 % пацієнтів з IIIB-IV стадіями
раку. Поліхіміотерапія вважається
основним методом лікування на IV стадії, хоча результати 5-річного виживання
цієї групи хворих дуже незначні -
1-5 %. Особливістю
дрібноклітинного раку є те, що після перших курсів хіміотерапії він стає
резистентним до цитостатиків і майже всі (90
%) пацієнти помирають
від рецидивування та метастазів, незважаючи на те, що спочатку була ремісія.
Обнадійливим препаратом другої лінії є Topotecan і його комбінація з Paclitaxel, які в окремих
дослідженнях були ефективними в 80-90 % випадках. Перспективними вважаються
методи генної терапії і вакцинотерапії, які інтенсивно розробляються. Профілактичне опромінення мозку (у 10 % випадків
спостерігається метастазування в мозок) рекомендується пацієнтам з обмеженим
дрібноклітинним раком легень, які отримали повну ремісію після хіміо-променевої
терапії. | |
|
| |
| Всього коментарів: 0 | |
| Copyright MyCorp © 2026 |
| Безкоштовний конструктор сайтів - uCoz |